иҫҫдјҜиҲ’жӯӨж¬Ўж–°йҖӮеә”з—ҮиҺ·жү№пјҢжҳҜеҹәдәҺдёӯеұұеӨ§еӯҰиӮҝзҳӨйҳІжІ»дёӯеҝғеј еҠӣж•ҷжҺҲзүөеӨҙзҡ„дёҖйЎ№еҸҢзӣІгҖҒйҡҸжңәеҜ№з…§IIIжңҹдёҙеәҠз ”з©¶вҖ”вҖ”иҫҫдјҜиҲ’®иҒ”еҗҲеҢ–з–—еҜ№жҜ”еҚ•зәҜеҢ–з–—з”ЁдәҺж— EGFRж•Ҹж„ҹзӘҒеҸҳжҲ–ALKеҹәеӣ йҮҚжҺ’зҡ„жҷҡжңҹжҲ–еӨҚеҸ‘жҖ§йқһйіһзҠ¶йқһе°Ҹз»ҶиғһиӮәзҷҢзҡ„дёҖзәҝжІ»з–—гҖӮз ”з©¶з»“жһңиЎЁжҳҺпјҢзӣёжҜ”еҚ•зәҜеҢ–з–—пјҢиҫҫдјҜиҲ’иҒ”еҗҲеҢ–з–—жҳҫ著延й•ҝдәҶж— иҝӣеұ•з”ҹеӯҳжңҹгҖӮ2020е№ҙ4жңҲпјҢеӣҪ家иҚҜе“Ғзӣ‘зқЈз®ЎзҗҶеұҖжӯЈејҸеҸ—зҗҶиҫҫдјҜиҲ’з”ЁдәҺйқһйіһзҠ¶йқһе°Ҹз»ҶиғһиӮәзҷҢдёҖзәҝжІ»з–—зҡ„йҖӮеә”з—Үз”іиҜ·гҖӮ2020е№ҙ8жңҲпјҢдҪңдёәе”ҜдёҖдёҖдёӘPD-1иҒ”еҗҲеҢ–з–—зҡ„з ”з©¶еңЁз¬¬21еұҠдё–з•ҢиӮәзҷҢеӨ§дјҡзәҝдёҠдё»йўҳи®әеқӣдёҠдә®зӣёгҖӮеҗҢж—¶пјҢиҝҷдёҖжҲҗжһңиў«еӣҪйҷ…иӮәзҷҢйўҶеҹҹзҹҘеҗҚжңҹеҲҠгҖҠJournal of Thoracic OncologyгҖӢйҖүдёӯпјҢеҗҢдёҖеӨ©еңЁзәҝеҸ‘иЎЁгҖӮ2жңҲ3ж—ҘпјҢеӣҪ家иҚҜе“Ғзӣ‘зқЈз®ЎзҗҶеұҖжӯЈејҸжү№еҮҶиҫҫдјҜиҲ’иҒ”еҗҲеҹ№зҫҺжӣІеЎһе’Ңй“Ӯзұ»еҢ–з–—йҖӮз”ЁдәҺиЎЁзҡ®з”ҹй•ҝеӣ еӯҗеҸ—дҪ“пјҲEGFRпјүеҹәеӣ зӘҒеҸҳйҳҙжҖ§е’Ңй—ҙеҸҳжҖ§ж·Ӣе·ҙзҳӨжҝҖй…¶пјҲALKпјүйҳҙжҖ§гҖҒдёҚеҸҜжүӢжңҜеҲҮйҷӨзҡ„еұҖйғЁжҷҡжңҹжҲ–иҪ¬з§»жҖ§йқһйіһзҠ¶йқһе°Ҹз»ҶиғһиӮәзҷҢпјҲNSCLCпјүжӮЈиҖ…зҡ„дёҖзәҝжІ»з–—гҖӮ
еӣҪйҷ…иӮәзҷҢйўҶеҹҹзҹҘеҗҚжңҹеҲҠгҖҠJournal of Thoracic OncologyгҖӢ
еҗҢж—ҘеңЁзәҝеҸ‘иЎЁдёҙеәҠдёүжңҹз ”з©¶з»“жһң
& M( N+ @. N- v) s, E; O% K( M' d- i* t# x; oдё–з•ҢеҚ«з”ҹз»„з»ҮеӣҪйҷ…зҷҢз—Үз ”з©¶жңәжһ„пјҲIARCпјүеҸ‘еёғзҡ„вҖң2020е№ҙе…ЁзҗғжңҖж–°зҷҢз—ҮиҙҹжӢ…ж•°жҚ®вҖқжҳҫзӨәпјҢиӮәзҷҢеҸ‘з—…зҺҮе…Ёдё–з•Ң第дәҢпјҢжӯ»дәЎзҺҮ第дёҖгҖӮиҖҢеңЁдёӯеӣҪпјҢиӮәзҷҢеҸ‘з—…зҺҮе’Ңжӯ»дәЎзҺҮеқҮжҺ’еҗҚ第дёҖгҖӮзәҰ70%зҡ„жӮЈиҖ…еңЁиҜҠж–ӯж—¶е·ІеҸ‘еұ•дёәдёҚйҖӮдәҺж №жІ»жҖ§жүӢжңҜзҡ„еұҖйғЁжҷҡжңҹжҲ–иҪ¬з§»жҖ§иӮәзҷҢгҖӮеҗҢж—¶пјҢеңЁжҺҘеҸ—жүӢжңҜжІ»з–—зҡ„ж—©жңҹжӮЈиҖ…дёӯпјҢд№ҹжңүзӣёеҪ“жҜ”дҫӢдјҡеҸ‘з”ҹеӨҚеҸ‘жҲ–иҝңеӨ„иҪ¬з§»гҖӮиӮәзҷҢж №жҚ®з»„з»ҮеӯҰзұ»еһӢеҲҶдёәе°Ҹз»ҶиғһиӮәзҷҢе’Ңйқһе°Ҹз»ҶиғһиӮәзҷҢпјҢе…¶дёӯйқһе°Ҹз»ҶиғһиӮәзҷҢзәҰеҚ 80%иҮі85%гҖӮдёӯеӣҪйқһе°Ҹз»ҶиғһиӮәзҷҢжӮЈиҖ…дёӯзәҰ70%дёәйқһйіһзҠ¶йқһе°Ҹз»ҶиғһиӮәзҷҢпјҢиҝҷе…¶дёӯжҺҘиҝ‘50%зҡ„жӮЈиҖ…ж— EGFRж•Ҹж„ҹзӘҒеҸҳжҲ–ALKеҹәеӣ йҮҚжҺ’пјҢдёҚйҖӮеҗҲйқ¶еҗ‘жІ»з–—пјҢжІ»з–—жүӢж®өжңүйҷҗпјҢеӯҳеңЁе·ЁеӨ§зҡ„жңӘиў«ж»Ўи¶ізҡ„дёҙеәҠйңҖжұӮгҖӮ
7 i$ X! j& O+ ?& k
е…Қз–«жІ»з–—жҳҜзҷҢз—ҮжІ»з–—йўҶеҹҹ继еҢ–з–—гҖҒж”ҫз–—гҖҒйқ¶еҗ‘жІ»з–—д№ӢеҗҺпјҢиҝ‘еҮ е№ҙжқҘзӮҷжүӢеҸҜзғӯзҡ„з ”з©¶йўҶеҹҹгҖӮPD-1жҠ‘еҲ¶еүӮеңЁе…Қз–«жІ»з–—йўҶеҹҹеӨҮеҸ—е…іжіЁпјҢйҖӮз”ЁдәҺеӨҡдёӘзҷҢз§ҚпјҢиў«з§°дёәвҖңе№ҝи°ұжҠ—зҷҢзҘһиҚҜвҖқгҖӮиҫҫдјҜиҲ’®жҳҜз”ұдҝЎиҫҫз”ҹзү©е’ҢзҫҺеӣҪзӨјжқҘе…ұеҗҢејҖеҸ‘гҖҒе…·жңүеӣҪйҷ…е“ҒиҙЁзҡ„еӣҪдә§PD-1жҠ‘еҲ¶еүӮпјҢдәҺ2018е№ҙ12жңҲеңЁдёӯеӣҪиҺ·жү№жІ»з–—еӨҚеҸ‘/йҡҫжІ»жҖ§з»Ҹе…ёеһӢйңҚеҘҮйҮ‘ж·Ӣе·ҙзҳӨпјҢжҳҜйҰ–дёӘеҲҠзҷ»еңЁжқғеЁҒеҢ»еӯҰжңҹеҲҠвҖ”вҖ”гҖҠжҹіеҸ¶еҲҖВ·иЎҖж¶ІеӯҰгҖӢзҡ„дёӯеӣҪе…Қз–«жІ»з–—дә§е“ҒгҖӮ2019е№ҙ11жңҲпјҢиҫҫдјҜиҲ’®жҲҗдёәе…ЁеӣҪйҰ–дёӘпјҢд№ҹжҳҜеҪ“е№ҙе”ҜдёҖдёҖдёӘиҝӣе…ҘеӣҪ家еҢ»дҝқзӣ®еҪ•зҡ„PD-1жҠ‘еҲ¶еүӮгҖӮ
2 ~# u/ h6 n# W5 AдёәдҪҝжӣҙеӨҡзҡ„жӮЈиҖ…иғҪеӨҹз”Ёеҫ—иө·й«ҳиҙЁйҮҸз”ҹзү©иҚҜпјҢдҝЎиҫҫз”ҹзү©иҒ”еҗҲдёӯеӣҪзҷҢз—ҮеҹәйҮ‘дјҡи®ҫз«ӢдәҶеҚ«з”ҹе…¬зӣҠжү¶иҙ«йЎ№зӣ®пјҢеҗ‘з¬ҰеҗҲжқЎд»¶зҡ„дҪҺдҝқжӮЈиҖ…е…Қиҙ№жҸҗдҫӣиҫҫдјҜиҲ’®пјҢи®©иҙ«еӣ°жӮЈиҖ…д№ҹиғҪжҺҘеҸ—еҲ°е…Ҳиҝӣзҡ„жІ»з–—ж–№жі•гҖӮдёәеҲҮе®һеҮҸиҪ»жӮЈиҖ…з»ҸжөҺиҙҹжӢ…пјҢ2021е№ҙ1жңҲпјҢдҝЎиҫҫз”ҹзү©е“Қеә”еҢ—дә¬еә·зӣҹеҹәйҮ‘дјҡдёәеӣ з—…иҮҙиҙ«зҡ„зҷҢз—ҮжӮЈиҖ…жҸҗдҫӣиҚҜе“Ғж•‘еҠ©зҡ„еҸ·еҸ¬пјҢеҸӮдёҺвҖңиҲ’еҝғеҸҜдҫқ-иӮҝзҳӨе…Қз–«жІ»з–—жӮЈиҖ…ж•‘еҠ©йЎ№зӣ®вҖқгҖӮ
' }( `2 e3 b' I. X% L* Q' D) y# KйЎ№зӣ®е·ІдәҺ1жңҲдёӯж—¬жӯЈејҸдёҠзәҝжҺҘеҸ—жӮЈиҖ…з”іиҜ·пјҢ并еңЁе…ЁеӣҪ230дёӘеҹҺеёӮзҡ„йЎ№зӣ®иҚҜеә—еҗҢжӯҘејҖеұ•пјҢдёәеӣҪеҶ…жҖҘйңҖиӮҝзҳӨе…Қз–«жІ»з–—иҚҜе“Ғзҡ„жӮЈиҖ…жҸҗдҫӣиҚҜе“Ғж•‘еҠ©гҖӮжҲӘжӯўзӣ®еүҚпјҢе·ІжңүжқҘиҮӘе…ЁеӣҪеҗ„дёӘеҹҺеёӮзҡ„ж•°еҚғеҗҚдҪҚжӮЈиҖ…пјҢйҖҡиҝҮз”өиҜқгҖҒеҫ®дҝЎзӯүжё йҒ“жҸҗдәӨз”іиҜ·пјҢ并йҷҶз»ӯиҺ·еҫ—ж•‘еҠ©гҖҒд»ҺдёӯеҸ—зӣҠгҖӮ
9 f. b+ F1 r4 R( F+ ^8 q
зҺ°жңүеӨҡз§Қж–№ејҸеҸҜиҺ·зҹҘйЎ№зӣ®з”іиҜ·иҜҰжғ…пјҡ
4 ?- f2 D2 b2 T: {, H1. еңЁеҫ®дҝЎдёӯжҗңзҙўвҖңиҲ’еҝғеҸҜдҫқвҖқпјҢе…іжіЁвҖңиҲ’еҝғеҸҜдҫқжӮЈиҖ…ж•‘еҠ©йЎ№зӣ®вҖқеҫ®дҝЎеҸ·пјҢзӣҙжҺҘиҺ·еҸ–иҜҰжғ…
0 Z4 l2 z. J* b' H: y, c" c: W8 C6 T- \9 j+ L- c
2. зҷ»еҪ•вҖңиҲ’еҝғеҸҜдҫқвҖқжӮЈиҖ…ж•‘еҠ©е…¬дј—еҸ·иҝӣиЎҢдёҖй”®з”іиҜ·пјҢе®ўжңҚдёҖеҜ№дёҖиҝӣиЎҢдё“дёҡжңҚеҠЎи§Јзӯ”
3. жӢЁжү“йЎ№зӣ®зғӯзәҝ010-58103659иҪ¬1е’ЁиҜўвҖңиҲ’еҝғеҸҜдҫқвҖқйЎ№зӣ®иҜҰз»ҶеҶ…е®№
# D* z# b' V6 V9 |: K, R
 3 M- S: L( z4 J) W1 @5 v8 v
3 M- S: L( z4 J) W1 @5 v8 v
. Q* d+ W. M0 T6 @5 r/ y0 hдёәдәҶи®©жӣҙеӨҡзҡ„жӮЈиҖ…еҸҜд»Ҙдә«еҸ—еҲ°е…Қз–«жІ»з–—еёҰжқҘзҡ„еҚ“и¶ҠдҪ“йӘҢпјҢвҖңиҲ’еҝғеҸҜдҫқ-жӮЈиҖ…ж•‘еҠ©йЎ№зӣ®вҖқз§үжүҝвҖңи®©жӮЈиҖ…жІ»з–—е…ЁзЁӢж— еҝ§вҖқзҡ„еҲқеҝғпјҢд»ҺеҲқжңҹд»·ж јй—Ёж§ӣе’ҢжҖ»жІ»з–—иҙ№з”ЁзӯүеӨҡз»ҙеәҰиҝӣиЎҢдәҶйҖҸеҪ»зҡ„и°ғз ”е’ҢзІҫеҝғзҡ„и®ЎеҲ’пјҢеҲҮе®һеё®еҠ©жӮЈиҖ…家еәӯеҮҸиҪ»з»ҸжөҺиҙҹжӢ…пјҢдә«еҸ—科жҠҖиҝӣжӯҘеёҰжқҘзҡ„еҒҘеә·жҲҗжһңпјҢ延з»ӯжӮЈиҖ…з”ҹе‘ҪеёҢжңӣгҖӮ
" m0 g5 s9 b: x6 J9 f% @! `) Oз¬ҰеҗҲйЎ№зӣ®ж•‘еҠ©иҢғеӣҙзҡ„жӮЈиҖ…пјҢж №жҚ®иҮӘиә«иҜүжұӮпјҢеҸҜиҮӘж„ҝеҸ‘иө·жұӮеҠ©з”іиҜ·пјҢз»Ҹе®Ўж ёйҖҡиҝҮеҗҺпјҢеҸҜжҢүд»ҘдёӢж–№жЎҲиҺ·еҫ—иҫҫдјҜиҲ’ж•‘еҠ©иҚҜе“Ғпјҡ
2 J0 k7 d+ h" E$ }% r
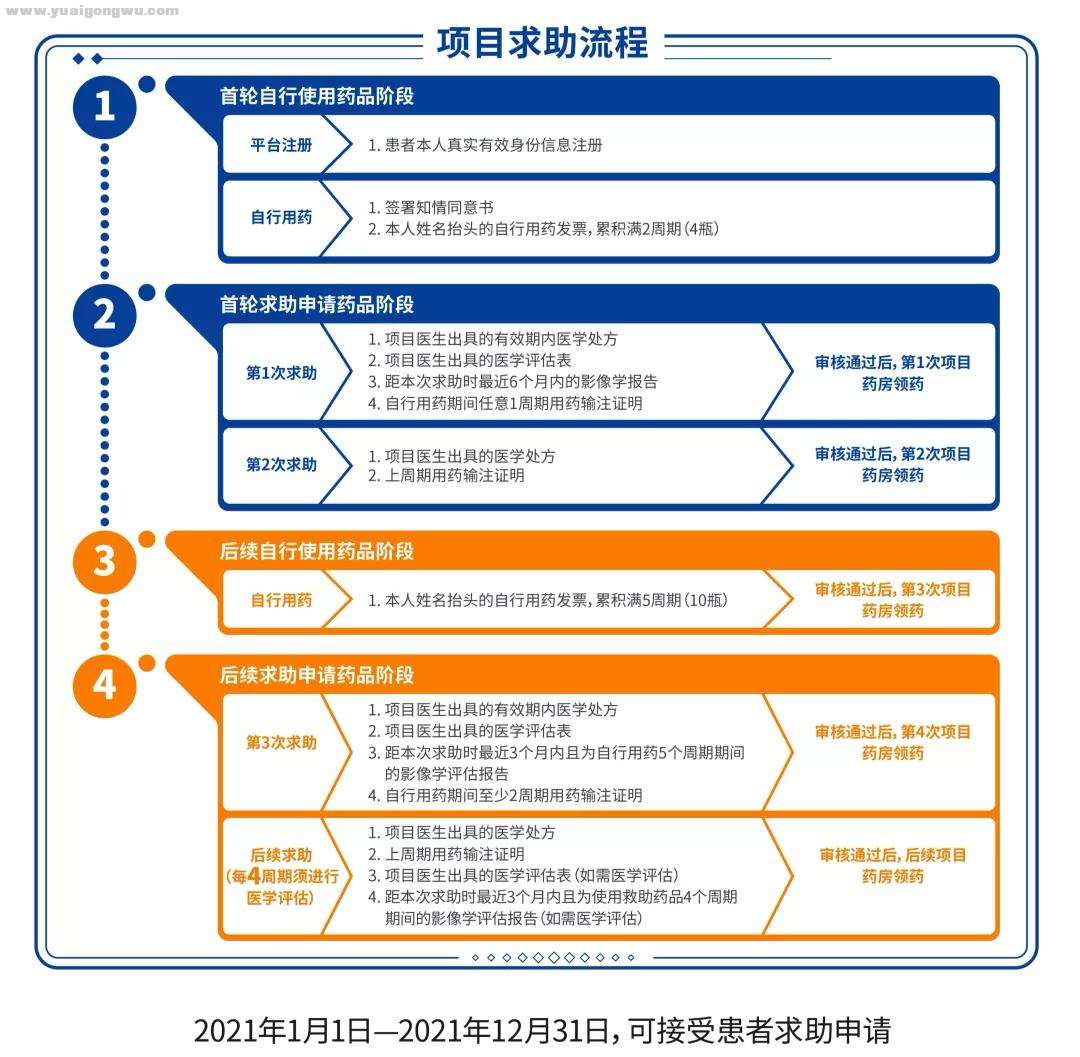
иҲ’еҝғеҸҜдҫқж•‘еҠ©ж–№жЎҲзӨәж„Ҹеӣҫ
* Y* j3 S O3 m0 B. R7 R1 n1 S
йҰ–иҪ®вҖң2+2вҖңеҚіиҙӯд№°2е‘ЁжңҹпјҲ4瓶пјүеҚіеҸҜиҺ·еҫ—2е‘ЁжңҹпјҲ4瓶пјүиҚҜе“Ғж•‘еҠ©пјҢеүҚеӣӣе‘Ёжңҹд»…ж”Ҝд»ҳ1.1дёҮе…ғпјӣеҗҺз»ӯвҖң5+NвҖқеҚіиҙӯд№°5е‘ЁжңҹпјҲ10瓶пјүеҸҜж•‘еҠ©иҮіз–ҫз—…иҝӣеұ•пјҢдҪҶзҙҜз§ҜдҪҝз”ЁиҫҫдјҜиҲ’жңҖеӨҡдёҚи¶…иҝҮ24дёӘжңҲпјҢж•ҙдёӘжІ»з–—жҖ»иҙ№з”Ё3.98дёҮе…ғе°ҒйЎ¶пјҢеҲҮе®һеё®еҠ©жӮЈиҖ…家еәӯеҮҸиҪ»з»ҸжөҺиҙҹжӢ…пјҢдә«еҸ—科жҠҖиҝӣжӯҘеёҰжқҘзҡ„еҒҘеә·жҲҗжһңпјҢ延з»ӯжӮЈиҖ…з”ҹе‘ҪеёҢжңӣгҖӮ
0 S3 v+ y& P$ @9 aдҪҺеҮҶе…Ҙй—Ёж§ӣпјҢ3.98дёҮе…ғе°ҒйЎ¶
) k2 X8 p$ L6 L/ e
е…Қз–«жІ»з–—ж–№жі•еҰӮPD-1жҠ‘еҲ¶еүӮд»Ҙе…¶зӢ¬зү№зҡ„дҪңз”ЁжңәеҲ¶пјҲйҖҡиҝҮжҝҖжҙ»дәәдҪ“иҮӘиә«е…Қз–«зі»з»ҹжқҘзҒӯжқҖиӮҝзҳӨз»ҶиғһпјүпјҢд»ҘдёӯеӣҪеҸ‘з—…зҺҮе’Ңжӯ»дәЎзҺҮжңҖй«ҳзҡ„зҷҢз—ҮиӮәзҷҢдёәдҫӢпјҢд»ҺеҢ…жӢ¬Keynote-001зӯүеҮ йЎ№еӨ§еһӢзҡ„дёҙеәҠз ”з©¶зҡ„дә”е№ҙз”ҹеӯҳж•°жҚ®дёӯзңӢеҮәпјҢйғЁеҲҶжӮЈиҖ…е·Із»Ҹе®һзҺ°дәҶй•ҝжңҹз”ҹеӯҳпјҢиҝҷд№ҹжҳҜе…Қз–«жІ»з–—иғҪйЈҺйқЎе…Ёзҗғзҡ„вҖңзҘһеҘҮвҖқжүҖеңЁгҖӮеҗҢж—¶пјҢе…Қз–«жІ»з–—жңүзӢ¬зү№й•ҝе°ҫж•Ҳеә”пјҢеҸҜйҮҚеҗҜжӮЈиҖ…зҡ„иӮҝзҳӨе…Қз–«еҫӘзҺҜпјҢд»ҺиҖҢдҪҝе…Қз–«и®°еҝҶдә§з”ҹжҸҗдҫӣй•ҝжңҹзҡ„е…Қз–«дҝқжҠӨзҡ„жҪңеҠӣпјҢиҝӣиҖҢдёәжӮЈиҖ…еёҰжқҘй•ҝжңҹзҡ„з”ҹеӯҳиҺ·зӣҠе’ҢжҢҒд№…зҡ„е…Қз–«еә”зӯ”гҖӮ
4 l$ T2 F8 X. N( V0 n$ ^1 _$ o; r
й—Ёж§ӣд»·дҪҺпјҡ1дёҮе…ғиҰҶзӣ–еүҚеӣӣе‘ЁжңҹпјҢеҚіеҸҜеҲқжӯҘиҜ„дј°PD-1з–—ж•Ҳ
7 o: X1 n& x% gиҷҪ然е…Қз–«жІ»з–—еёҰз»ҷжӮЈиҖ…зҡ„жғҠе–ңйҮҚйҮҚпјҢдҪҶ并дёҚжҳҜжүҖжңүжӮЈиҖ…йғҪйҖӮеҗҲе…Қз–«жІ»з–—гҖӮеҰӮдҪ•еҲӨж–ӯе…Қз–«жІ»з–—жҳҜеҗҰжңүж•ҲйңҖиҰҒжңүдёҖдёӘиҜ•й”ҷзҡ„иҝҮзЁӢгҖӮд»ҺејҖе§ӢдҪҝз”ЁPD-1жҠ‘еҲ¶еүӮпјҢеҲ°йҰ–ж¬ЎеӨҚжҹҘеҶіе®ҡжӮЈиҖ…еҗҺз»ӯжҳҜеҗҰйҖӮеҗҲ继з»ӯз”ЁиҚҜпјҢдјҡдә§з”ҹдёҖйғЁеҲҶиҙ№з”ЁпјҢиҝҷе°ұжҳҜе…Қз–«жІ»з–—зҡ„й—Ёж§ӣиҙ№з”ЁгҖӮиҝҷдёҖиҙ№з”ЁжҳҜжӮЈиҖ…йҖүжӢ©е…Қз–«жІ»з–—еүҚйңҖиҰҒзҹҘйҒ“зҡ„第дёҖдёӘе…ій”®жҖ§д»·ж јгҖӮ
: h+ d4 h5 P: ~# pж №жҚ®дёҙеәҠиҜ•йӘҢж•°жҚ®жқҘзңӢпјҢжӮЈиҖ…дҪҝз”Ёе…Қз–«жІ»з–—иө·ж•Ҳж—¶й—ҙзәҰдёә2-4дёӘе‘ЁжңҹпјҢд№ҹе°ұжҳҜиҜҙпјҢжӮЈиҖ…еңЁ3дёӘжңҲпјҲ4дёӘжІ»з–—е‘Ёжңҹпјүж—¶е°ұеҸҜд»ҘйҖҡиҝҮеҪұеғҸеӯҰжЈҖжҹҘе°ұдәҶи§Је…Қз–«жІ»з–—еҜ№иҮӘе·ұжҳҜеҗҰжңүж•ҲгҖӮжң¬ж¬ЎиҲ’еҝғеҸҜдҫқзҡ„йЎ№зӣ®пјҢд»…1.1дёҮе…ғеҚіиҰҶзӣ–PD-1жІ»з–—еүҚ4дёӘе‘ЁжңҹпјҢеӨ§е№…еәҰйҷҚдҪҺжӮЈиҖ…зҡ„жңҹеҲқз”ЁиҚҜжҲҗжң¬гҖӮ
8 u+ I1 F3 }$ G8 A5 z+ \е…ЁзЁӢж— еҝ§пјҡеҜ№дәҺй•ҝжңҹжңүж•Ҳзҡ„жӮЈиҖ…пјҢиҚҜе“Ғж•‘еҠ©иҮіз–ҫз—…иҝӣеұ•пјҢе°ҒйЎ¶24дёӘжңҲ
2 H1 n2 U) E( q, g* Q" N& x- n
еңЁеҜ№е…Қз–«жІ»з–—ж•ҲжһңжңүдәҶеҲқжӯҘзҡ„еҲӨж–ӯеҗҺпјҢеҰӮжһңд»ҺдёӯеҸ—зӣҠеҶіе®ҡ继з»ӯдҪҝз”Ёе…Қз–«жІ»з–—пјҢдҪ иҝҳеҸҜд»Ҙ继з»ӯдә«еҸ—вҖңеҗҺз»ӯ5+NвҖқзҡ„иҚҜе“Ғж•‘еҠ©пјҢиҙӯд№°5дёӘе‘ЁжңҹеҗҺзӣҙиҮіз–ҫз—…иҝӣеұ•жҲ–з”Ёж»Ў24дёӘжңҲпјҢеңЁиҝҷжңҹй—ҙж— йңҖеҶҚиҠұй’ұд№°иҚҜпјҢж•ҙдёӘжІ»з–—жҖ»иҙ№з”Ё3.98дёҮе…ғе°ҒйЎ¶гҖӮ
1 i0 K' P# _4 d8 }дёҖй”®з”іиҜ· е…ЁеӣҪиҰҶзӣ– й•ҝжңҹж”ҜжҢҒ
: @$ V3 C' `2 r
жҲӘиҮізӣ®еүҚпјҢеӣҪеҶ…е·Іжңүе…«ж¬ҫе…Қз–«иҚҜе“ҒиҺ·жү№дёҠеёӮпјҢиҖҢдҪңдёәе”ҜдёҖдёҖж¬ҫеҗҲиө„дә§е“ҒпјҢиҫҫдјҜиҲ’жӯӨж¬Ўж”ҜжҢҒзҡ„ж•‘еҠ©йЎ№зӣ®еҗҢж—¶еңЁжҖ§д»·жҜ”е’Ңж“ҚдҪңжҖ§д№ҹд»ҘжӮЈиҖ…дёәдёӯеҝғиҝӣиЎҢдәҶеӨҡж–№иҖғйҮҸгҖӮж—ўиҰҒеңЁз»ҸжөҺдёҠж”ҜжҢҒпјҢд№ҹеёҢжңӣиғҪз®ҖеҢ–жӮЈиҖ…家еәӯж“ҚдҪңгҖӮжӮЈиҖ…еҸҜд»ҘеңЁеҢ»иҚҜзӯ№е№іеҸ°иҝӣиЎҢдёҖй”®з”іиҜ·пјҢе®ўжңҚдёҖеҜ№дёҖиҝӣиЎҢдё“дёҡжңҚеҠЎиҖҗеҝғи§Јзӯ”гҖӮж“ҚдҪңз®ҖдҫҝпјҢз”іиҜ·дҫҝжҚ·пјҢзӣ®еүҚе…ЁеӣҪеӨҡең°е·ІжңүжӮЈиҖ…йўҶиҚҜпјҢз”іиҜ·иҝҳеңЁжҢҒз»ӯиҝӣиЎҢдёӯгҖӮ
, f' b: B9 Q1 E& H# y
йҰ–дҪҚеҸ—зӣҠжӮЈиҖ…е·ІдәҺ1жңҲ29ж—ҘеңЁдёҠжө·йўҶиҚҜ
5 n. w4 t5 X4 G: V' [ ^, ?жӯӨж¬ЎвҖңиҲ’еҝғеҸҜдҫқ-жӮЈиҖ…ж•‘еҠ©йЎ№зӣ®вҖқд»Һеҗ„дёӘз»ҙеәҰе…ЁйқўиҜ„дј°дәҶжӮЈиҖ…зҡ„е®һйҷ…з»ҸжөҺеҺӢеҠӣпјҢеҲҮе®һжҸҗдҫӣдәҶж“ҚдҪңдҫҝжҚ·гҖҒж”ҜжҢҒеҠӣеәҰеӨ§зҡ„ж•‘еҠ©ж–№жЎҲгҖӮиҚҜзү©еҸҜеҸҠжҖ§зҡ„жҸҗй«ҳжҳҜиҚҜзү©е®һзҺ°д»·еҖјгҖҒи®©жӮЈиҖ…иҺ·зӣҠзҡ„йҮҚиҰҒдёҖзҺҜпјҢжҲ‘们еёҢжңӣи¶ҠжқҘи¶ҠеӨҡзҡ„жӮЈиҖ…иғҪеӨҹеҫ—зӣҠдәҺеҢ»з–—科еӯҰиҝӣжӯҘпјҢз”Ёеҫ—дёҠгҖҒз”Ёеҫ—иө·й«ҳиҙЁйҮҸзҡ„з”ҹзү©иҚҜпјҢиҺ·еҫ—ж–°з”ҹгҖӮ
7 \) U: [2 Y" c0 u+ w- zйҷӨдәҶеҲҡеҲҡиҺ·жү№зҡ„иӮәйқһйіһзҷҢд№ӢеӨ–пјҢдҝЎиҫҫз”ҹзү©жӯЈеҠӘеҠӣжӢ“еұ•иҫҫдјҜиҲ’®зҡ„йҖӮеә”з—ҮиҢғеӣҙпјҢеңЁе…ЁзҗғиҢғеӣҙеҶ…ејҖеұ•дәҶ20еӨҡйЎ№е…ідәҺиҫҫдјҜиҲ’®зҡ„дёҙеәҠз ”з©¶гҖӮйҷӨдәҶе·Із»ҸиҺ·жү№дёҠеёӮзҡ„дёӨдёӘйҖӮеә”з—ҮеӨ–пјҢиҫҫдјҜиҲ’дёҖзәҝе’ҢдәҢзәҝжІ»з–—йіһзҠ¶йқһе°Ҹз»ҶиғһиӮәзҷҢпјҢд»ҘеҸҠдёҖзәҝжІ»з–—иӮқзҷҢзҡ„дёҠеёӮз”іиҜ·еқҮе·Іиў«еӣҪ家иҚҜе“Ғзӣ‘зқЈз®ЎзҗҶеұҖеҸ—зҗҶгҖӮжӯӨеӨ–пјҢйЈҹз®ЎзҷҢгҖҒз»“зӣҙиӮ зҷҢгҖҒиғғзҷҢгҖҒиғҶз®ЎзҷҢгҖҒе®«йўҲзҷҢгҖҒж·Ӣе·ҙзҳӨгҖҒй»‘иүІзҙ зҳӨзӯүйўҶеҹҹдёҙеәҠз ”з©¶д№ҹеңЁиҝӣиЎҢдёӯгҖӮ
' h7 I2 t* u( F+ q/ z
д»Ҡе№ҙдё–з•ҢзҷҢз—Үж—Ҙзҡ„дё»йўҳжҳҜпјҡвҖңе…ізҲұжӮЈиҖ…пјҢе…ұеҗҢжҠ—зҷҢвҖқпјҢдҝЎиҫҫз”ҹзү©з”ЁиЎҢеҠЁи·өиЎҢзқҖиҝҷдёҖеҖЎеҜјгҖӮд»Һ2011е№ҙжҲҗз«Ӣд№ӢеҲқпјҢдҝЎиҫҫз”ҹзү©е°ұзЎ®е®ҡдәҶејҖеҸ‘еӣҪйҷ…ж ҮеҮҶзҡ„й«ҳиҙЁйҮҸз”ҹзү©еҲӣж–°иҚҜзҡ„зӣ®ж ҮпјҢйҖҡиҝҮе»әи®ҫеӣҪйҷ…еҢ–дә§дёҡеҹәең°гҖҒеј•иҝӣеӣҪйҷ…дәәжүҚгҖҒејҖеұ•еӣҪйҷ…еҗҲдҪңпјҢзЎ®дҝқејҖеҸ‘зҡ„жҜҸдёҖж¬ҫдә§е“ҒйғҪиҫҫеҲ°еӣҪйҷ…ж ҮеҮҶпјҢе…·жңүеӣҪйҷ…е“ҒиҙЁпјҢ并дәүеҸ–йқўеҗ‘жӣҙе№ҝйҳ”зҡ„еӣҪйҷ…еёӮеңәгҖӮ2020е№ҙ3жңҲпјҢ欧жҙІиҚҜзү©з®ЎзҗҶеұҖ(EMA)е’ҢзҫҺеӣҪйЈҹе“Ғе’ҢиҚҜзү©з®ЎзҗҶеұҖ(FDA)е…ҲеҗҺжҺҲдәҲиҫҫдјҜиҲ’еӯӨе„ҝиҚҜиө„ж јпјҢйҖӮеә”з—ҮеҲҶеҲ«дёәеӨ–е‘ЁTз»Ҷиғһж·Ӣе·ҙзҳӨе’ҢTз»Ҷиғһж·Ӣе·ҙзҳӨпјӣ4жңҲпјҢFDAеҶҚж¬ЎжҺҲдәҲиҫҫдјҜиҲ’еӯӨе„ҝиҚҜиө„ж јпјҢз”ЁдәҺжІ»з–—йЈҹз®ЎзҷҢпјӣ5жңҲпјҢдҝЎиҫҫз”ҹзү©дёҺзҫҺеӣҪеҫ·е·һеӨ§еӯҰMDе®үеҫ·жЈ®зҷҢз—Үдёӯеҝғе®ЈеёғиҫҫжҲҗжҲҳз•ҘеҗҲдҪңпјҢеҸҢж–№е°ҶеңЁзҫҺеӣҪејҖеҸ‘иҫҫдјҜиҲ’®з”ЁдәҺжІ»з–—еӨҡз§ҚзҪ•и§ҒзҷҢз—ҮгҖӮ2020е№ҙ8жңҲпјҢдҝЎиҫҫз”ҹзү©дёҺзҫҺеӣҪзӨјжқҘеҲ¶иҚҜ第еӣӣж¬ЎиҫҫжҲҗжҲҳз•ҘеҗҲдҪңпјҢжҺҲдәҲзӨјжқҘиҫҫдјҜиҲ’еңЁдёӯеӣҪең°еҢәеӨ–ең°зҡ„зӢ¬е®¶и®ёеҸҜпјҢе°ҶиҫҫдјҜиҲ’жҺЁеҗ‘е…ЁзҗғпјҢи®©дёӯеӣҪеҲӣж–°иҚҜиө°еҗ‘дё–з•ҢпјҢйҖ зҰҸе…Ёзҗғзҷҫ姓гҖӮ
6 z3 h, o! Y. c' s" F$ W7 P4 R
жҲҗз«ӢеҚҒе№ҙпјҢдҝЎиҫҫз”ҹзү©е·Із»Ҹе»әз«Ӣиө·дёҖжқЎеҢ…жӢ¬23дёӘж–°иҚҜе“Ғз§Қзҡ„дә§е“Ғй“ҫпјҢйҷӨдәҶиҫҫдјҜиҲ’пјҢиҝҳдәҺ2020е№ҙдёҠеёӮдәҶдёүж¬ҫеҲӣж–°иҚҜвҖ”вҖ”иҫҫж”ёеҗҢгҖҒиҫҫдјҜеҚҺгҖҒиӢҸз«ӢдҝЎпјҢжҲҗдёәжӢҘжңүеҚ•жҠ—иҚҜе“ҒдёҠеёӮж•°йҮҸжңҖеӨҡзҡ„дёӯеӣҪдјҒдёҡпјҢд№ҹжҳҜе…ЁзҗғеҺҶеҸІдёҠе”ҜдёҖдёҖ家еҲӣеҠһд№қе№ҙеҚіжңүеӣӣдёӘеҚ•жҠ—дә§е“ҒдёҠеёӮзҡ„иҚҜдјҒгҖӮжҚ®жӮүпјҢдҝЎиҫҫз”ҹзү©еҸҲдёҖж¬ЎжҠҠзӣ®е…үиҒҡз„Ұз”ҹзү©еҲӣж–°иҚҜзҡ„жңҖеүҚжІҝпјҢеҠӘеҠӣејҖеҸ‘е…Ёзҗғе…Ёж–°йқ¶зӮ№(First-in-class)иҚҜзү©пјҢзӣ®еүҚжүҝиҪҪиҝҷдёҖеҲӣж–°зӣ®ж Үзҡ„е…Ёзҗғз ”еҸ‘е№іеҸ°дҝЎиҫҫеӣҪжё…йҷўе·Із»ҸжӯЈејҸжҲҗз«ӢгҖӮ2020е№ҙ10жңҲпјҢдҝЎиҫҫз”ҹзү©д»»е‘Ҫз”ҹзү©еҢ»иҚҜиЎҢдёҡдё–з•Ңи‘—еҗҚ科еӯҰ家еҲҳеӢҮеҶӣеҚҡеЈ«дёәйӣҶеӣўжҖ»иЈҒпјҢиҙҹиҙЈйӣҶеӣўе…Ёзҗғз ”еҸ‘гҖҒз®ЎзәҝжҲҳз•ҘгҖҒе•ҶеҠЎеҗҲдҪңеҸҠеӣҪйҷ…дёҡеҠЎзӯүе·ҘдҪңгҖӮеҲҳеҚҡеЈ«е°ҶйўҶеҜјеӣҪжё…йҷўдҪңдёәдҝЎиҫҫејәжңүеҠӣзҡ„ж–°иҚҜз ”еҸ‘еј•ж“ҺпјҢеңЁжңӘжқҘ5-10е№ҙеҶ…е®һзҺ°е…¬еҸёе…Ёзҗғе…Ёж–°йқ¶зӮ№(First-in-class)дә§е“Ғзҡ„дёҠеёӮгҖӮ
. L- h6 l& Y: w" @. o: P7 u7 R7 E
. h9 Q: `! ~% V& J: V
w! @- |, y. Y1 n

